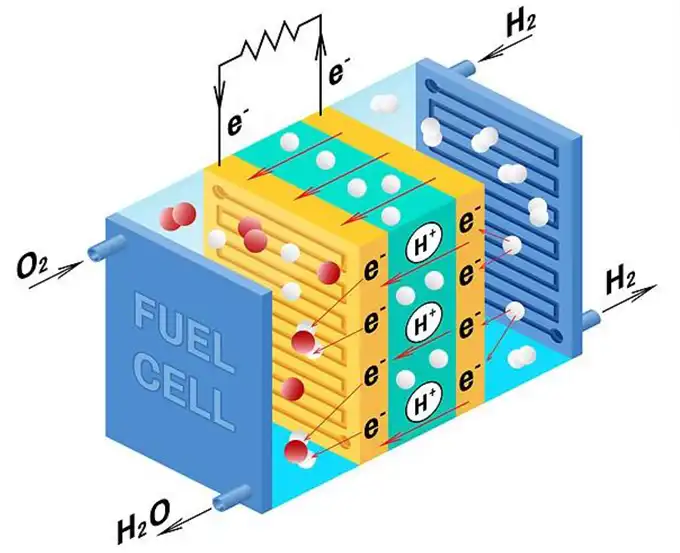
Da sich die weltweite Energielandschaft verändert und die Ziele des „Carbon Peaking“ und der „Kohlenstoffneutralität“ vorgeschlagen werden, hat Wasserstoffenergie, mit der höchsten Massenergiedichte und null Kohlenstoffemissionen, zunehmende Aufmerksamkeit erlangt. Protonenaustauschmembran-Brennstoffzellen (PEMFCs) sind derzeit eine sehr vielversprechende Wasserstoffenergienutzungstechnologie aufgrund ihrer niedrigen Betriebstemperatur, schnellen Start-up-Zeit und ihrer Umweltfreundlichkeit, was sie in vielen Bereichen wie Luft- und Raumfahrt, Seefahrt, Automobilen, stationären Stromquellen und vielen anderen weit verbreitet anwendbar macht.
Notiz: Die praktische Anwendung von Proton Austausch Membran-Brennstoffzellen
Bis heute bleiben platinbasierte Katalysatoren die primäre Wahl für Katalysatoren in PEMFCs aufgrund ihrer überlegenen Sauerstoff reduktionsreaktion (ORR) und Wasserstoffoxidationsreaktion (HOR) Leistung. Platin ist jedoch ein seltenes und kostbares Metall, und seine hohen Kosten schränken die Kommerzialisierung von Brennstoffzellen ein. Laut der Prognose des US-Energieministeriums (DOE) für 2022 werden bei einer jährlichen Lieferung von 50.000 PEMFC-Stapeln die Katalysatorkosten 59% der gesamten Produktionskosten der Stapel ausmachen.
Die Sauerstoff reduktionsreaktion (ORR) ist einer der Kernschritte im gesamten elektrochemischen Prozess und hat einen entscheidenden Einfluss auf die Ausgangsspannung und Effizienz von Brennstoffzellen. Allerdings ist die Katalysatormenge für die ORR relativ hoch und wird auf mehr als 80% der gesamten Menge geschätzt. Zudem ist ihre Rückbildungsfähigkeit schlecht, die Polarisierung ist stark, und der kinetische Prozess ist ein komplexer Vier-Elektronen-Prozess. Verschiedene Zwischenprodukte sind an der Reaktion beteiligt, wie H2O2 und sauerstoffhaltige adsorbierte Zwischenprodukte (O2,ad und OHad, etc.). Diese Zwischenprodukte verursachen ein Überspannungspotential im ORR-Prozess von bis zu 0,2 V oder sogar höher. Daher ist die Entwicklung hochaktiver ORR-Katalysatoren mit geringem Platingehalt entscheidend, um die großflächige Anwendung von Brennstoffzellen zu fördern.
Derzeit gibt es zahlreiche Berichte über den ORR-Mechanismus und experimentelle Forschungen, die jedoch alle leicht variieren. Diese umfassen:
Zwei-Elektronen-Weg: Dies umfasst hauptsächlich zwei primäre Schritte: die partielle Reduktion des Sauerstoffmoleküls zur Erzeugung von Wasserstoffperoxid, das dann weiter zu Wasser reduziert wird. Dieser Mechanismus kann durch die folgenden Schritte dargestellt werden:
O2 + 2H+ + 2e– → H2O2
H2O2 + 2H+ + 2e– → 2H2O
Dieser Weg wird auch als Zwei-Stufen-Vier-Elektronen-Prozess bezeichnet, wobei Wasserstoffperoxid (H2O2) das Zwischenprodukt ist. Das Vorhandensein von Wasserstoffperoxid kann zu einer Katalysatorvergiftung und Effizienzreduzierung führen.
Sequenzieller Einzelelektronen-Weg: In diesem Weg erfolgt die Reduktion des Sauerstoffmoleküls durch aufeinanderfolgende Einzelelektronen-Übertragungsschritte, wobei jeweils ein Einzelelektronen-Zwischenprodukt gebildet wird, wie:
O2+e–→O2–
O2–+e–→O22-
O22-+e–→2O–
2O–+4H++2e–→2H2O
Dieser Weg umfasst mehrere Einzelelektronen-Übertragungsschritte und produziert verschiedene Zwischenprodukte, die den Reaktionsprozess komplizieren.
Direkter Vier-Elektronen-Weg: Dies ist der ideale Reaktionsweg, da er die Bildung schädlicher Zwischenprodukte vermeidet und das Sauerstoffmolekül direkt zu Wasser reduziert:
O2+4H++4e–→2H2O
Stufenweiser Vier-Elektronen-Weg: In diesem Weg kann der Sauerstoffreduktionsprozess in mehrere kleinere Schritte unterteilt werden, wobei jeweils schrittweise Protonen und Elektronen hinzugefügt werden und verschiedene Zwischenprodukte gebildet werden:
O2+H++e–→HO2
HO2+H++e–→H2O2
H2O2+H++e–→HO+H2O
HO+H++e–→H2O
Dieser Weg veranschaulicht die schrittweise Addition von Protonen und Elektronen sowie die Bildung und Umwandlung verschiedener Zwischenprodukte.
Die obigen Erklärungen drehen sich hauptsächlich um theoretische Studien zum „Vier-Elektronen-Prozess“. Es gibt viele andere unterschiedliche theoretische Studien, die hier nicht im Detail behandelt werden. Die verschiedenen Forschungstheorien zur Sauerstoff reduktionsreaktion (ORR) zeigen die Komplexität und Vielfalt der Reaktionswege, wobei der direkte Vier-Elektronen-Prozess der idealste Weg ist.
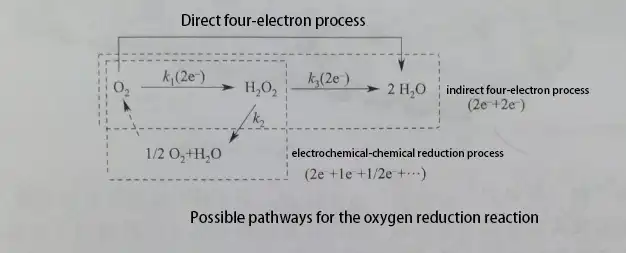
Im direkten Vier-Elektronen-Reaktionsprozess adsorbiert O2 zuerst auf der Oberfläche des Elektrokatalysators und bildet adsorbierten Sauerstoff. Der adsorbierte Sauerstoff reagiert durch verschiedene Wege: Wenn der adsorbierte Sauerstoff direkt elektrochemisch über den Vier-Elektronen-Weg zu H2O reduziert wird, nennt man dies den „direkten Vier-Elektronen-Prozess“. Wenn der adsorbierte Sauerstoff das Zwischenprodukt H2O2 über den Zwei-Elektronen-Weg bildet und H2O2 direkt von der Katalysatoroberfläche desorbiert, nennt man dies den „Zwei-Elektronen-Reduktionsprozess“. Wenn H2O2 weiter zu H2O reduziert wird, nennt man dies den „indirekten Vier-Elektronen-Prozess“ oder „H2O2-Prozess“. Wenn H2O2 auf der Oberfläche des Elektrokatalysators (katalytisch oder chemisch) zu H2O und O2 zersetzt wird und das resultierende O2 die O2-Reduktionsreaktion fortsetzt, nennt man diesen Prozess den „elektrochemischen-chemischen Reduktionsprozess“.
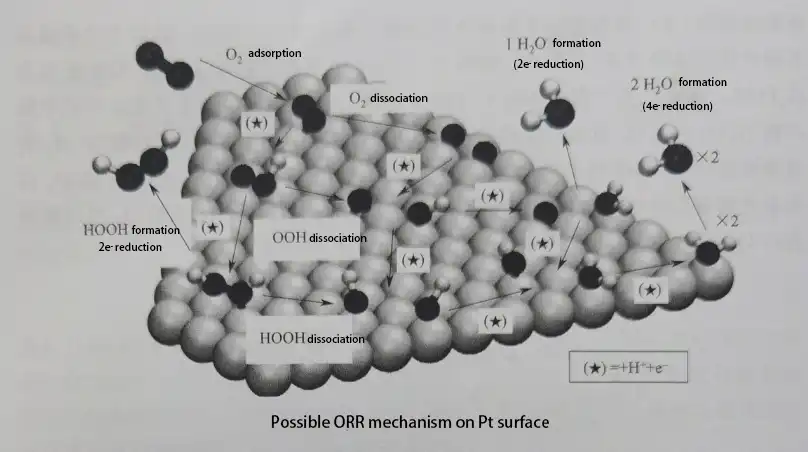
ORR-Mechanismus auf der Pt-Oberfläche
Der komplexe ORR-Prozess umfasst mehrere Schritte der Elektronen- und Protonenübertragung. Durch das Studium dieses Prozesses kann man die geschwindigkeitsbestimmenden Schritte der ORR-Kinetik ermitteln und die Ursachen für das Überspannungspotential identifizieren. Daher ist das Verständnis des ORR-Prozesses auf atomarer Ebene entscheidend für die Gestaltung von Hochleistungselektrokatalysatoren. Es wurde umfangreiche Forschung zu den Reaktionsmechanismen der ORR auf verschiedenen Elektrokatalysatoroberflächen durchgeführt, wobei Pt/C nach wie vor einer der Elektrokatalysatoren mit hoher ORR-Katalyseaktivität ist. Folglich wurde der Reduktionsreaktionsmechanismus von O2 auf der Pt-Elektrokatalysatoroberfläche am intensivsten untersucht.
Es gibt ein umfassendes Verständnis der Beziehung zwischen ORR-Reaktionskinetik und den elektronischen Eigenschaften von Metalloberflächen. Zukünftige Forschung muss jedoch kontinuierlich vertieft werden, um effizientere und stabilere ORR-Katalysatoren zu entwickeln. Die Forschung zum ORR-Mechanismus kann wie folgt zusammengefasst werden:
Erstens diffundiert O2 zur Elektrokatalysatoroberfläche und bildet adsorbierte Sauerstoffmoleküle (O2*, wobei * aktive Stellen auf der Katalysatoroberfläche repräsentiert). Basierend auf den O-O-Bindungsbruchschritten kann der Reduktionsmechanismus von O2* in drei Wege unterteilt werden:
Dissoziativer Weg: Die O-O-Bindung bricht direkt, um O*-Zwischenprodukte zu bilden, die anschließend zu OH* und H2O* reduziert werden.
Assoziativer Weg: O2* wird zuerst zu OOH* reduziert. Dann bricht die O-O-Bindung in OOH*, um O* und OH*-Zwischenprodukte zu bilden, die weiter reduziert werden.
Peroxid-Weg (sekundärer assoziativer Weg): O2* wird nacheinander zu OOH* und HOOH* reduziert, bevor die O-O-Bindung bricht, um OH* zu bilden. Die Zwischenprodukte werden weiterhin reduziert.
Zwischenprodukte wie O*, OOH* und OH* sind entscheidend im ORR-Prozess. Direkte experimentelle Beweise für diese Zwischenprodukte sind schwer zu erhalten, aber theoretische Berechnungen haben substanzielle Beweise geliefert. Forscher haben mithilfe von Dichtefunktionaltheorie (DFT)-Berechnungen gezeigt, dass die Adsorption von Sauerstoffspezies auf der Elektrokatalysatoroberfläche die Ursache für das Überspannungspotential ist. Bei hohen Spannungen sind auf der Elektrokatalysatoroberfläche adsorbierte Sauerstoffspezies stabil, was den Protonen- und Elektronentransfer erschwert. Wenn die Spannung sinkt, nimmt die Stabilität des adsorbierten Sauerstoffs ab und die Oxidationsreaktion kann stattfinden.
Die Bindungsenergie zwischen Sauerstoffspezies und der Elektrokatalysatoroberfläche bestimmt direkt die katalytische Aktivität des Elektrokatalysators. Für einen hochaktiven Elektrokatalysator sollte die Bindungsenergie zwischen der Oberfläche und den Zwischenprodukten angemessen sein: Wenn die Adsorptionsbindungsenergie zu schwach ist, wird der Transfer von Elektronen und Protonen zum adsorbierten Sauerstoff behindert; ist die Adsorptionsbindungsenergie zu stark, wird das produzierte H2O schwer desorbierbar, wodurch aktive Stellen besetzt werden und eine weitere Adsorption von O2 verhindert wird, was die ORR-Aktivität des Elektrokatalysators verringert.
Der grundlegende Grund für den Unterschied in der Bindungsenergie zwischen Zwischenprodukten und verschiedenen Elektrokatalysatoroberflächen liegt in der elektronischen Struktur relativ zum Fermi-Niveau (dem höchsten besetzten Orbital). Je höher die Position des Metall-d-Bandes, desto stärker die Wechselwirkung zwischen der Elektrokatalysatoroberfläche und den Zwischenprodukten. Daher wird, wenn die Bindungsenergie zwischen den Zwischenprodukten und dem Elektrokatalysator angemessen ist, die elektronische Struktur optimiert, was zu einer höheren ORR-Katalyseaktivität führt.
Die Beziehung zwischen der Bindungsenergie von adsorbierten Spezies (O*, OOH*, OH*) auf verschiedenen Metall-Elektrokatalysatoroberflächen und der Sauerstoffreduktionsaktivität bildet eine „Vulkan-Plot“. Unter vielen Metallen hat Pt im Vergleich zu anderen Metallen (wie Fe, Co, Ni usw.) eine relativ geeignete Bindungsenergiestärke mit O*, OOH* und OH*, was zu einer hohen ORR-Aktivität führt.
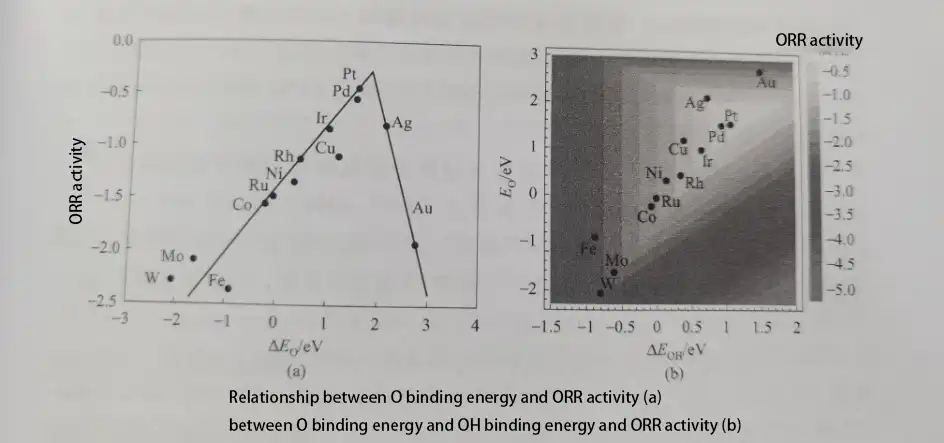
Laut diesem Plot ist die Bindungsenergie zwischen Pt und adsorbiertem Sauerstoff nicht die optimalste, aber ein Elektrokatalysator mit etwas schwächerer Bindungsenergie als Pt würde eine höhere ORR-Aktivität aufweisen. Konkret wird der Elektrokatalysator die höchste ORR-Aktivität haben, wenn die Adsorptionsbindungsenergie um 0,2 eV schwächer ist als bei Pt.
Sauerstoff reduktionsreaktion von Nicht-Edelmetall-Elektrokatalysatoren
Die Anwendung von Nicht-Edelmetall-Elektrokatalysatoren in der Sauerstoff reduktionsreaktion (ORR) ist aufgrund ihrer geringen Kosten und reichhaltigen Ressourcen von großer Bedeutung. Obwohl bedeutende Fortschritte beim Studium des ORR-Mechanismus von Nicht-Edelmetall-Katalysatoren (NPMCs) gemacht wurden, hauptsächlich in Laborumgebungen, ist kontinuierliche, vertiefte Forschung notwendig, um viele technische Herausforderungen zu bewältigen und eine großflächige Anwendung zu erreichen. Hier sind einige wichtige Fortschritte und Forschungsschwerpunkte in diesem Bereich:
Materialdesign und -synthese:
Forscher verbessern die ORR-Aktivität und -Haltbarkeit durch das Design und die Synthese neuartiger Nicht-Edelmetall-Katalysatoren. Beispielsweise haben aus metallorganischen Gerüsten (MOF) abgeleitete kohlenstoffbasierte Katalysatoren und stickstoffdotierte Kohlenstoffmaterialien (Fe-N-C, Co-N-C) eine hohe katalytische Leistung gezeigt.
Strukturcharakterisierung und Mechanismusanalyse:
Fortschrittliche Charakterisierungstechniken wie Röntgenabsorptionsspektroskopie (XAS), Transmissionselektronenmikroskopie (TEM), Rasterelektronenmikroskopie (REM) und Röntgenphotoelektronenspektroskopie (XPS) werden verwendet, um die Mikrostruktur und Oberflächeneigenschaften der Katalysatoren zu untersuchen. Diese Techniken helfen, die aktiven Stellen, katalytischen Mechanismen und Abbaupfade der Katalysatoren zu verstehen.
Theoretische Berechnungen und Simulationen:
Dichtefunktionaltheorie (DFT) und Molekulardynamik (MD)-Simulationen spielen eine entscheidende Rolle beim Verständnis des ORR-Mechanismus. Durch rechnerische Simulationen können Forscher aktive Stellen, Reaktionspfade und Energiebarrieren vorhersagen, was das Design und die Optimierung von Katalysatoren leitet.
Praktische Anwendung und Leistungsevaluation:
Leistungstests von Nicht-Edelmetall-Katalysatoren in praktischen Anwendungen wie Brennstoffzellen und Lithium-Luft-Batterien sind ein wichtiger Forschungsschwerpunkt. Langzeitstabilitätstests und Leistungsevaluationen unter realen Betriebsbedingungen überprüfen die Praktikabilität und Zuverlässigkeit der Katalysatoren.
Abbaumechanismusforschung:
Um die Haltbarkeit von Nicht-Edelmetall-Katalysatoren zu verbessern, erforschen Forscher die Mechanismen des Katalysatorabbaus. Das Verständnis der Ursachen des Abbaus, wie Metallionenauslaugung und Korrosion der Kohlenstoffmatrix, hilft bei der Gestaltung stabilerer Katalysatoren.
ORR-Mechanismus von Nicht-Edelmetall-Elektrokatalysatoren:
Für Übergangsmetall-Stickstoff-Kohlenstoff-Katalysatoren (M-N-C) glauben Forscher, dass ihre katalytischen Mechanismen ähnlich sind. Am Beispiel von Fe-N-C beginnt die ORR, die durch Fe-N-C katalysiert wird, mit zweiwertigem Fe, das unter sauren Bedingungen als N4FeII-OH2 beginnen könnte. O2 adsorbiert auf N4FeII-OH2, während es ein Elektron und ein Proton aufnimmt, wie in der folgenden Gleichung gezeigt: :N4FeII-OH2-OH2+O2+H++e–→N4FeIII-O-OH+H2O. Die Reaktion kann dann über zwei Wege verlaufen:
Weg 1:
N4FeIII– O – OH nimmt ein Proton und ein Elektron auf, gibt ein Wassermolekül ab und bildet eine hochvalente Fe-Oxo-Spezies. Es nimmt weiterhin Elektronen und Protonen auf und kehrt schließlich zur hydratisierten zweiwertigen Fe-Form zurück. Die spezifischen Schritte sind wie folgt:
(1) N4FeIII-O-OH+H++e–→N4FeIV=O+H2O
(2) N4FeIV=O+H++e–→N4FeIII-OH
(3) N4FeIII-OH+H++e–→N4FeII-OH2
Weg 2:
N4FeIII-O-OH nimmt ein Proton und ein Elektron auf, um H2O2 zu bilden, und die katalytische aktive Stelle kehrt nach Adsorption eines Wassermoleküls zur hydratisierten zweiwertigen Eisenform zurück, wie folgt:
(1) N4FeIII-O-OH+H++e–→N4FeII+H2O2
(2) N4FeII+H2O→N4FeII-OH2
Im Weg 1 nimmt O2 direkt vier Protonen und vier Elektronen auf, was dem direkten Vier-Elektronen-Weg der ORR entspricht. Dieser Weg erfordert die Bildung eines vierwertigen Fe-Zwischenprodukts. Im Weg 2 nimmt O2 nur zwei Protonen und zwei Elektronen auf, was dem Zwei-Elektronen-Weg der ORR entspricht. Einige Forscher schlagen vor, dass vierwertiges Fe bei durch Fe-N-C katalysierter ORR möglich ist, aber nur unter hohen Überspannungen. Dies könnte erklären, warum Fe-N-C-Katalysatoren bei hohen Überspannungen einem direkten Vier-Elektronen-Weg und bei niedrigen Spannungen einem Zwei-Elektronen-Weg folgen. Gemäß dieser Ansicht, da CoN4 weniger wahrscheinlich hochvalente Co-Zustände bildet, folgt die durch CoN4 katalysierte ORR typischerweise dem Zwei-Elektronen-Weg und erzeugt H2O2.
Schlussfolgerung:
Während sich das globale Energieparadigma in Richtung Nachhaltigkeit verschiebt und die Ziele „CO2-Peak“ und „CO2-Neutralität“ gesetzt werden, rückt Wasserstoffenergie, insbesondere durch Protonenaustauschmembran-Brennstoffzellen (PEMFCs), als zentrale Technologie in den Vordergrund. Trotz der Herausforderungen, die durch die Abhängigkeit von platinbasierten Katalysatoren entstehen, ebnen bedeutende Fortschritte im Verständnis der Sauerstoff reduktionsreaktion (ORR) und der Entwicklung von Nicht-Edelmetall-Katalysatoren (NPMCs) den Weg für effizientere und kostengünstigere Lösungen. Durch die kontinuierliche Erforschung und Innovation im Bereich des Katalysatordesigns, der Synthese und des mechanistischen Verständnisses können wir das volle Potenzial der Wasserstoffenergie erschließen und ihren breiten kommerziellen Einsatz vorantreiben. Diese Reise, gekennzeichnet durch rigorose Forschung und technologische Durchbrüche, verspricht eine sauberere und nachhaltigere Energiezukunft.
Verwandte Artikel:
Electrode Reactions in Fuel Cells: Anode and Cathode