วิธีการหาค่าประสิทธิภาพที่แม่นยำเป็นสิ่งสำคัญในการศึกษาประสิทธิภาพของตัวเร่งปฏิกิริยาไฟฟ้า บทความนี้จะกล่าวถึงวิธีทดสอบประสิทธิภาพของตัวเร่งปฏิกิริยาไฟฟ้าทั่วไปหลายวิธี รวมถึงวิธีแบตเตอรี่เดี่ยว (Single battery), อิเล็กโทรดจานหมุน (RDE) และอิเล็กโทรดจานหมุนวงแหวน (RRDE), โวลแทมเมตรีแบบรอบ (CV) และโวลแทมเมตรีแบบกวาดเชิงเส้น (LSV) แต่ละวิธีมีข้อดีและขอบเขตการใช้งานที่เฉพาะเจาะจง การเข้าใจหลักการพื้นฐานและการประยุกต์ใช้ของวิธีเหล่านี้จะช่วยให้สามารถประเมินประสิทธิภาพของตัวเร่งปฏิกิริยาไฟฟ้าได้อย่างครบถ้วนและแม่นยำมากขึ้น ส่งเสริมการวิจัยในเซลล์เชื้อเพลิงและการใช้งานทางเคมีไฟฟ้าอื่น ๆ
แบตเตอรี่เดี่ยว (Single battery)
วิธีสำคัญอย่างหนึ่งในการหาค่าประสิทธิภาพของตัวเร่งปฏิกิริยาไฟฟ้าคือการผสมตัวเร่งปฏิกิริยาไฟฟ้า, แอลกอฮอล์, น้ำ และเรซินนำโปรตอนในอัตราส่วนที่เหมาะสมเพื่อสร้างสารละลาย จากนั้นสารละลายนี้จะถูกพ่นหรือแปรงบนเมมเบรนแลกเปลี่ยนโปรตอนหรือชั้นกระจายแก๊ส และได้อิเล็กโทรดเมมเบรนโดยการกดร้อน ประสิทธิภาพการเร่งปฏิกิริยาจะถูกประเมินโดยใช้วิธีแบตเตอรี่เดี่ยว ซึ่งสามารถเปรียบเทียบตัวเร่งปฏิกิริยาไฟฟ้าต่าง ๆ ได้
วิธีนี้มีประสิทธิภาพสูง โดยเฉพาะในด้านการวิจัยเซลล์เชื้อเพลิง เนื่องจากสามารถประเมินประสิทธิภาพทางเคมีไฟฟ้าของตัวเร่งปฏิกิริยาในสภาพการทำงานจริงและพิจารณาปัจจัยต่าง ๆ เช่น การกระจายตัวของตัวเร่งปฏิกิริยาในอิเล็กโทรดเมมเบรน, การนำโปรตอน, และการแพร่กระจายของแก๊ส อย่างไรก็ตาม สภาพการเตรียมอิเล็กโทรดเมมเบรนมีผลกระทบต่อการประเมินประสิทธิภาพของตัวเร่งปฏิกิริยาไฟฟ้าอย่างมาก วิธีแบตเตอรี่เดี่ยววัดประสิทธิภาพโดยรวมของตัวเร่งปฏิกิริยาไฟฟ้า แต่ไม่อนุญาตให้ทำการวิจัยเชิงลึกเกี่ยวกับกลไกการเร่งปฏิกิริยาบนผิวของตัวเร่งปฏิกิริยาไฟฟ้า
วิธีอิเล็กโทรดจานหมุนและอิเล็กโทรดจานหมุนวงแหวน (RDE และ RRDE)
อิเล็กโทรดจานหมุน (RDE) และอิเล็กโทรดจานหมุนวงแหวน (RRDE) เป็นสองวิธีการทดสอบทางเคมีไฟฟ้าที่ใช้กันทั่วไปสำหรับการประเมินประสิทธิภาพของตัวเร่งปฏิกิริยาไฟฟ้า วิธีเหล่านี้สามารถประเมินประสิทธิภาพทางเคมีไฟฟ้าเบื้องต้นของตัวเร่งปฏิกิริยาไฟฟ้า เช่น กิจกรรม, ความเสถียร, และกลไกปฏิกิริยาได้ในเวลาอันสั้น เหมาะสำหรับการศึกษากลไกของปฏิกิริยาเคมีไฟฟ้า เช่น ปฏิกิริยาลดออกซิเจน (ORR) โดยการควบคุมความเร็วในการหมุน วิธีเหล่านี้สามารถควบคุมกระบวนการถ่ายเทมวลได้อย่างแม่นยำ ทำให้ได้สภาวะการทดสอบที่เสถียรและสามารถทำซ้ำได้สูง
อิเล็กโทรดจานหมุนวงแหวน (RRDE): เป็นเทคนิคการวัดทางเคมีไฟฟ้าที่พัฒนาจาก RDE และเหมาะสมเป็นพิเศษสำหรับการตรวจสอบผลิตภัณฑ์กลางในปฏิกิริยาเคมีไฟฟ้า หากเกิดปฏิกิริยาลดบนอิเล็กโทรดจาน ผลิตภัณฑ์กลางที่เกิดขึ้นจะถูกพาโดยการไหลของสารละลายไปยังอิเล็กโทรดวงแหวน โดยการใช้ศักย์ไฟฟ้าต่ออิเล็กโทรดวงแหวนที่สามารถออกซิไดซ์ผลิตภัณฑ์กลาง กระแสปฏิกิริยาออกซิเดชันสามารถถูกตรวจจับบนอิเล็กโทรดวงแหวน ทำให้สามารถศึกษาวิถีทางปฏิกิริยาและการสร้างและการบริโภคผลิตภัณฑ์กลางได้
เมื่อเทียบกับวิธีแบตเตอรี่เดี่ยว RDE และ RRDE เหมาะสมกว่าสำหรับการประเมินประสิทธิภาพเบื้องต้นและการศึกษากลไกปฏิกิริยา ในขณะที่วิธีแบตเตอรี่เดี่ยวให้การประเมินประสิทธิภาพโดยรวมของตัวเร่งปฏิกิริยาในสภาพการทำงานจริงมากขึ้น สำหรับการทดสอบ ORR อัตราการผลิต H2O2 และจำนวนการถ่ายเทอิเล็กตรอน (n) ระหว่างกระบวนการลดออกซิเจนบนตัวเร่งปฏิกิริยาไฟฟ้าสามารถคำนวณได้โดยใช้สูตรต่อไปนี้:
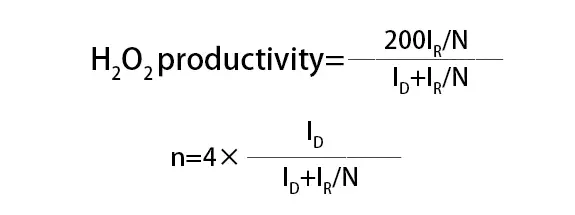
ซึ่ง ID เป็นกระแสไฟฟ้าของฟาราเดย์บนอิเล็กโทรดจาน, IR เป็นกระแสไฟฟ้าของฟาราเดย์บนอิเล็กโทรดวงแหวน, และ N เป็นประสิทธิภาพการเก็บรวบรวมของอิเล็กโทรดจานสำหรับ H2O2
โวลแทมเมตรีแบบรอบ (CV)
โวลแทมเมตรีแบบรอบ (CV) เป็นวิธีการทดลองทางเคมีไฟฟ้าแบบทรานเซียนต์ที่ใช้กันอย่างแพร่หลายในการศึกษากลไกและพลศาสตร์ของปฏิกิริยา โดยการควบคุมศักย์ไฟฟ้าของอิเล็กโทรดให้สแกนในรูปแบบคลื่นสามเหลี่ยมในอัตราที่ต่างกันตามเวลา เกิดปฏิกิริยาลดและออกซิเดชันสลับกันบนอิเล็กโทรด และบันทึกกราฟกระแส-ศักย์ไฟฟ้า ที่เรียกว่ากราฟโวลแทมเมตร
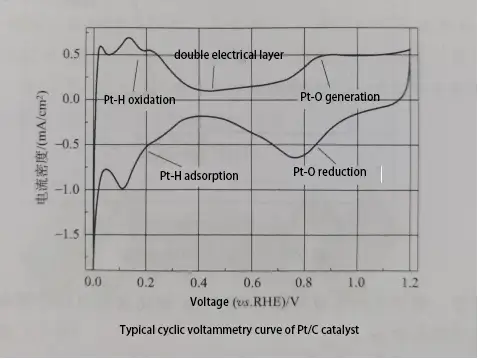
รูปแสดงกราฟ CV ที่เป็นแบบฉบับสำหรับตัวเร่งปฏิกิริยา Pt/C แบ่งเป็นห้าส่วน: ยอดการดูดซับไฮโดรเจน, บริเวณชั้นสองชั้น, ยอดออกซิเดชันของพื้นผิว Pt, ยอดลด Pt ออกไซด์, และยอดการสลายไฮโดรเจน จากกราฟการสลายไฮโดรเจนบนอิเล็กโทรด Pt ในกราฟ CV สามารถคำนวณพื้นที่ผิวที่มีปฏิกิริยาทางเคมีไฟฟ้าที่แอคทีฟ (ECSA) ของตัวเร่งปฏิกิริยาไฟฟ้าได้ ซึ่งเป็นพื้นที่ผิวที่มีปฏิกิริยาทางเคมีไฟฟ้าต่อมวลของแพลตินัม หน่วยเป็น m²/g สูตรการคำนวณคือ:
ECSA=Q/(mC)
Q=S/u
ซึ่ง Q คือประจุรวมของยอดการสลายไฮโดรเจนในกราฟ CV หลังจากลบชั้นสองชั้นออก, m คือการโหลดของ Pt บนขั้วไฟฟ้า, C คือค่าความจุการดูดซับของชั้นบางของไฮโดรเจนบนผิว Pt (210μC/cm²), S คือพื้นที่รวมของยอดการสลายไฮโดรเจนในกราฟ CV, และ u คืออัตราการสแกนระหว่างการทดสอบ CV ECSA เป็นหนึ่งในพารามิเตอร์สำคัญสำหรับการประเมินตัวเร่งปฏิกิริยาพลาตินัมเบส
โวลแทมเมตรีแบบกวาดเชิงเส้น (LSV)
โวลแทมเมตรีแบบกวาดเชิงเส้น (LSV) เกี่ยวข้องกับการใช้สัญญาณสแกนศักย์ไฟฟ้าเชิงเส้น (ซึ่งศักย์ไฟฟ้าเปลี่ยนแปลงเชิงเส้นกับเวลา) ระหว่างขั้วไฟฟ้าทำงานและขั้วไฟฟ้าอ้างอิง ขณะเดียวกันวัดกระแสที่ไหลระหว่างขั้วไฟฟ้าทำงานและขั้วไฟฟ้าช่วยเพื่อให้ได้กราฟโพลาไรเซชัน กราฟโพลาไรเซชันสำหรับปฏิกิริยาลดออกซิเจน (ORR) ทั่วไปสามารถแบ่งออกเป็นสามส่วน: บริเวณควบคุมโดยพลศาสตร์, บริเวณควบคุมแบบผสมระหว่างพลศาสตร์และการแพร่กระจาย, และบริเวณควบคุมการแพร่กระจาย
บริเวณควบคุมโดยพลศาสตร์: ในบริเวณนี้ อัตราปฏิกิริยา ORR ค่อนข้างช้า ส่งผลให้กระแสเล็กน้อยหรือแทบไม่มีการเปลี่ยนแปลง เมื่อศักย์ไฟฟ้าลดลง ความหนาแน่นของกระแสจะเพิ่มขึ้นช้า ๆ
บริเวณควบคุมแบบผสมระหว่างพลศาสตร์และการแพร่กระจาย: เมื่อศักย์ไฟฟ้าลดลงต่อไป อัตราปฏิกิริยา ORR เร่งขึ้น ซึ่งแสดงให้เห็นโดยความหนาแน่นของกระแสที่เพิ่มขึ้นอย่างมีนัยสำคัญเมื่อศักย์ไฟฟ้าลดลง ในบริเวณนี้ อัตรา ORR ถูกกำหนดโดยทั้งอัตราพลศาสตร์ของปฏิกิริยาและอัตราการแพร่กระจายของออกซิเจน
บริเวณควบคุมการแพร่กระจาย: ในบริเวณนี้ อัตราพลศาสตร์ของปฏิกิริยาเกินกว่าอัตราการแพร่กระจายของออกซิเจน ซึ่งหมายความว่าอัตราการลดออกซิเจนบนผิวของตัวเร่งปฏิกิริยาฟ้าเกินกว่าอัตราการแพร่กระจายของออกซิเจนจากอิเล็กโทรไลต์จำนวนมากมายังผิวของตัวเร่งปฏิกิริยาฟ้า ดังนั้นอัตรา ORR ถูกควบคุมโดยอัตราการแพร่กระจายของออกซิเจน และกราฟโพลาไรเซชันในบริเวณนี้จะสร้างระดับความหนาแน่นกระแสที่จำกัด ซึ่งความหนาแน่นของกระแสไม่เปลี่ยนแปลงตามศักย์ไฟฟ้า
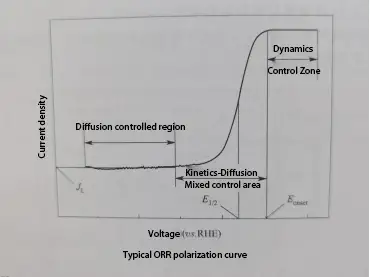
ในกราฟโพลาไรเซชัน ORR สองพารามิเตอร์สามารถบ่งบอกถึงกิจกรรมการเร่งปฏิกิริยาไฟฟ้าของตัวเร่งปฏิกิริยา: ศักย์เริ่มต้น (Eonset) และศักย์ครึ่งคลื่น (E1/2)
ศักย์เริ่มต้น (Eonset):
ศักย์เริ่มต้นเป็นค่าศักย์ไฟฟ้าที่ขอบเขตระหว่างบริเวณควบคุมโดยพลศาสตร์และบริเวณควบคุมแบบผสมระหว่างพลศาสตร์และการแพร่กระจายในกราฟโพลาไรเซชัน วิธีการวัดต่าง ๆ ถูกใช้ในการศึกษาต่าง ๆ รวมถึง:
ค่าศักย์ไฟฟ้าที่ 5% ของความหนาแน่นกระแสที่จำกัด
ค่าศักย์ไฟฟ้าที่ความหนาแน่นกระแส 0.1 mA/cm²
การตัดกันของเส้นสัมผัสที่จุดความชันสูงสุดในบริเวณควบคุมแบบผสมระหว่างพลศาสตร์และการแพร่กระจายกับความหนาแน่นกระแสเป็นศูนย์
ศักย์ครึ่งคลื่น (E1/2):
ศักย์ครึ่งคลื่นเป็นค่าศักย์ไฟฟ้าที่ความหนาแน่นกระสเท่ากับครึ่งหนึ่งของความหนาแน่นกระแสที่จำกัด พารามิเตอร์นี้สะท้อนถึงกิจกรรมการเร่งปฏิกิริยาปานกลางของตัวเร่งปฏิกิริยาไฟฟ้าใน ORR
ในการคำนวณจำนวนอิเล็กตรอนที่ถูกถ่ายโอนในระหว่างกระบวนการ ORR สำหรับความเร็วในการหมุนของอิเล็กโทรดต่าง ๆ ใช้สมการ Koutecky-Levich (K-L):
1/ID=1/IK+1/(Bw1/2)
ซึ่ง ID คือกระแสที่วัดได้, IK คือกระแสพลศาสตร์, w คือความเร็วในการหมุนของอิเล็กโทรด (rpm หรือ rad/s), และ B คือค่าสมการกลับของความชันที่คำนวณโดยใช้สมการ Levich:
B=0,62nFAC0D02/3u-1/6
ซึ่ง n คือจำนวนอิเล็กตรอนที่ถูกถ่ายโอนต่อโมเลกุลของออกซิเจน, F คือค่าคงที่ของฟาราเดย์ (96485 C/mol), D0 คือค่าสัมประสิทธิ์การแพร่กระจายของ O2, C0 คือความเข้มข้นของ O2 ในอิเล็กโทรไลต์, และ ν คือความหนืดจลน์ของอิเล็กโทรไลต์
การแนะนำข้างต้นแสดงให้เห็นถึงการประยุกต์ใช้ที่สำคัญของวิธีการทดสอบประสิทธิภาพตัวเร่งปฏิกิริยาฟ้าต่าง ๆ ในการวิจัยเคมีไฟฟ้า โดยการใช้วิธีเหล่านี้ร่วมกัน นักวิจัยสามารถหาค่าประสิทธิภาพของตัวเร่งปฏิกิริยาฟ้าได้แม่นยำมากขึ้น ส่งเสริมการพัฒนาเทคโนโลยีเซลล์เชื้อเพลิงและการประยุกต์ใช้เคมีไฟฟ้าอื่น ๆ

